Unidad 4 Alcanos
Grupo de compuestos formados por carbono e hidrógeno, las uniones carbono-carbono se realizan por enlaces sencillos que forman grandes cadenas carbonadas. En los inicios de su estudio fueron llamados parafinas, de latín que significa poca afinidad.
En los alcanos al sustituir un hidrógeno de su cadena carbonada por un halógeno (cloro, bromo, flúor y yodo), obtenemos un derivado halogenado.
Ejemplo:

Los alcanos tienen gran utilidad para el hombre ya que hacen parte constitutiva de la gasolina (pentano y hexano) y del gas natural (metano, etano y propano)
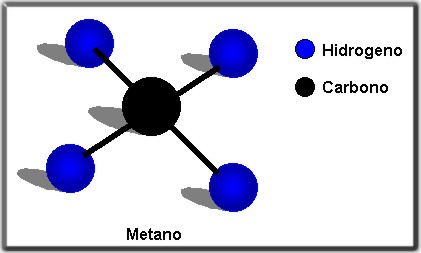
Cuando un alcano pierde un hidrogeno se transforma en un radical alquílico. Los radicales poseen una terminación il.
Ejemplo:

4.2 Nomenclatura de alcanos
Para nombrar los alcanos utilizamos las reglas de la IUPAC, como prefijos utilizamos (met, et, prop, but, et, pent, de acuerdo al numero de carbonos que constituyen la cadena carbonada. Como sufijo utilizamos la terminación ano.
Ejemplo:
Alcanos de cadena no ramificada:
CH4 Metano (Met: Significa que en la estructura existe un solo carbono y ano nos indica que la unión carbono hidrógeno se realiza mediante enlaces sencillos).
CH3-CH3 Etano (Et. Significa que la estructura presenta dos carbonos y ano nos indica que los enlaces carbono-carbono e hidrógeno carbono son sencillos).
Para nombrar los alcanos ramificados utilizamos algunas reglas de la IUPAC que anotaremos a continuación.
Alcanos de cadena ramificada:
- Escogemos la cadena más larga
y la llamamos principal.
- Se numera la cadena principal
buscando que los carbonos con sustituyente posean el número más pequeño
posible.
- Nombrar los sustituyentes indicando el carbono que lo posee mediante un número (ubicación en la cadena).
Ejemplo:
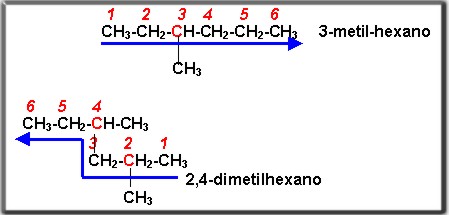
La dirección de la flecha indica el sentido correcto de la numeración.
4. En algunas ocasiones la estructura presenta más de un sustituyente en la cadena utilizamos di, tri, tetra, si existen dos, tres o cuatro sustituyentes en la cadena carbonada.

4.3 Propiedades físicas
Estas dependen del número, estructura y clase de átomos que constituyen la molécula. Son compuestos neutros, de densidad menor que uno, con estados físicos sólidos, líquidos y gaseosos.

El punto de ebullición se ve influenciado por el peso molecular ya que a medida que aumenta el peso molecular aumenta el punto de ebullición.

Son insolubles en el agua y solubles en compuestos tales como alcohol y el éter.
4.4 Propiedades
químicas
Los alcanos son poco reactivos debido a la unión de las moléculas por enlaces sigma que son fuertes y difíciles de romper; sin embargo, presentan algunas reacciones tales como:
Reacción en la cual cambiamos uno o varios hidrógenos por los halógenos correspondientes (excepción del yodo).

Sustitución de un átomo de hidrogeno por un grupo nitro (-NO2) a una temperatura de 450 grados centígrados.
Ejemplo:

Los nitroalcanos son utilizados como disolventes y combustibles.
4.4.3 Oxidación
Los alcanos al reaccionar con el oxígeno (arden) producen gas carbónico, agua y calor.
![]()
La cantidad de calor producida varía con el número de carbonos que posee el alcano.
4.5 Obtención de alcanos
4.5.1 Hidrólisis del reactivo de Grignard
El reactivo de Grignard es un compuesto de formula general R-Mg-X, donde R es un radical alquílico o aromático, Mg magnesio y X es un elemento halógeno. Recibe el nombre en honor al descubridor Víctor Grignard la hidrólisis consiste en agregar agua al reactivo de Grignard.
Ejemplo:
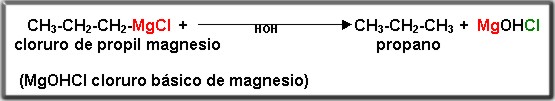
4.5.2 Síntesis de Wurtz (creada por Adolfo Wurtz)
Reacción de un haluro de alquilo con sodio para producir un alcano y una sal.

4.5.3 Hidrogenación catalítica de alquenos
Reacción en la que agregamos hidrógeno en presencia de un catalizador (níquel, paladio, platino) a un alqueno.
Ejemplo:

4.5.4 Proceso de Fischer-Tropsch
En esta reacción el monóxido de carbono es sometido a hidrólisis catalítica, para producir un alcano.
![]()
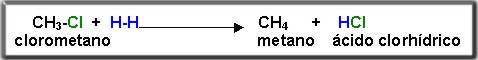
4.5.5 Reducción de halogenuros de alquilo
Consiste en agregar hidrógenos a un halogenuro de alquilo.
4.6 Usos de los
alcanos
Utilizados como combustibles en estufas. Encendedores y disolventes.
