Unidad 3 Nomenclatura y Reacciones orgánicas
3.1 Nomenclatura
Los primeros nombres de los compuestos orgánicos tomaban como base la sustancia que los contenía.
Ejemplo:
- El ácido láctico: se le denominó así por encontrarse en la leche.
- El ácido cítrico: aislado de las frutas cítricas.
- El ácido fórmico: se aisló de las hormigas (fórmica, en latín).
- El metano: inicialmente se denominó gas de los pantanos.

ALGUNAS FRUTAS CONTIENEN
ÁCIDO CITRICO
Hacia el año 1924 en Amsterdam nace la Unión Internacional de Química Pura y Aplicada IUPAC (International Union of Pure and Appliqued Chemestry), que determinara las reglas lógicas para la nomenclatura de compuestos orgánicos.
3.1.1 Reglas generales
de nomenclatura
Para nombrar un compuesto orgánico se debe identificar:
1. El tipo de cadena: lineal, ramificada o cíclica
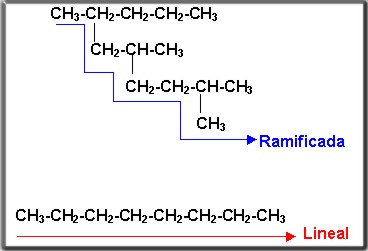
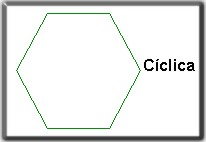
2. El número de átomos de carbono
a. Raíz o prefijo: indica el número de átomos de carbono que constituyen
la molécula, la cual se puede expresar en forma estructural mostrando el tipo
de enlace o abreviada.
b. Sufijo primario ó terminación: corresponde al tipo de función.
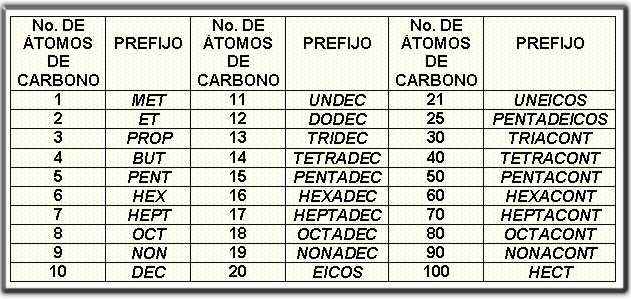
Tabla de prefijos utilizados
para nombrar compuestos orgánicos.
Por ejemplo, para nombrar el más sencillo de los alcanos se tiene:
a. Raíz: corresponde met: 1 átomo de carbono
b. Sufijo primario: corresponde a la terminación ano: por tratarse de la función alcano
Luego, su nombre es metano y su representación es la siguiente:
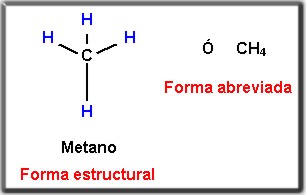
3. Tipo de función química
De acuerdo a la función las terminaciones más comunes son:
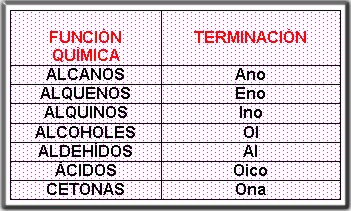
Ejemplos:

3.2 Mecanismos de las reacciones orgánicas

MUCHAS REACCIONES ORGANICAS
SUCEDEN EN EL APACIBLE MUNDO DE LA NATURALEZA.
Los pasos químicos o transformaciones que sufre un reactivo orgánico para transformarse en producto es conocido como mecanismo de reacción. El mecanismo de reacción nos permite entender de manera química las etapas y constituyentes de cada una de las moléculas que entran en reacción.
En las reacciones orgánicas tenemos en cuenta dos términos:
3.2.1 Sustrato: Compuesto o grupo de compuestos que en su estructura posee el carbono.
3.2.2 Reactivo: Compuesto generalmente inorgánico que ataca el sustrato
puede ser:
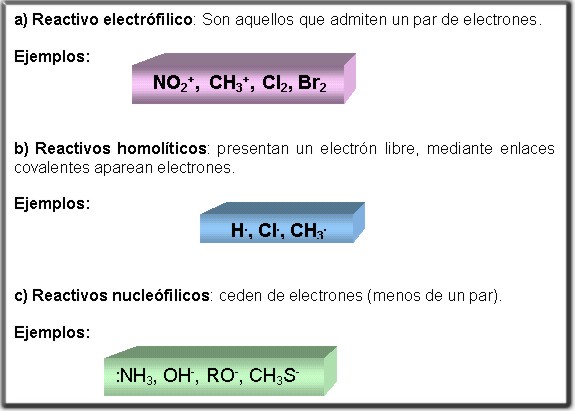
3.2.3 Tipos de
ruptura orgánica
Durante las reacciones orgánicas hay ruptura y formación de enlaces químicos (transformaciones de la materia). La ruptura se puede originar de dos maneras:
3.2.3.1 Heterolítica: Los electrones son llevados por uno de los átomos que entran en reacción.
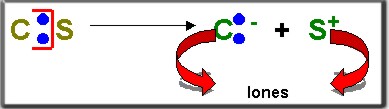
Para comprender mejor la ruptura observemos el siguiente ejemplo donde el metano origina dos iones.
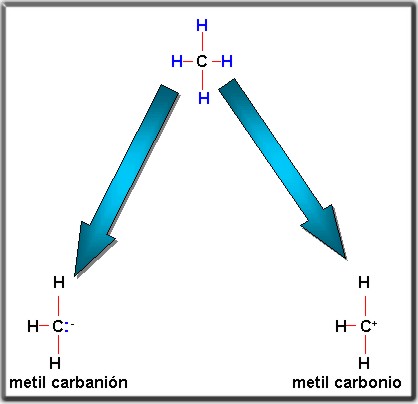
3.2.3.2 Homolítica: Los átomos se reparten igual numero de electrones y originan radicales.
Ejemplo:
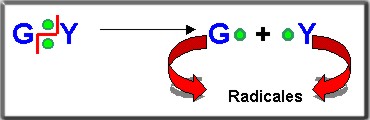
Para entender mejor la ruptura homolitica observemos el siguiente ejercicio.

