Unidad 1. Historia de la química orgánica y características del carbono
Química orgánica es la ciencia que estudia los compuestos que poseen el elemento carbono en su estructura.
EL CARBONO ESTRUCTURA DE
LOS COMPUESTOS ORGÁNICOS
Además del carbono, estos compuestos tienen otros elementos como:
- Hidrógeno: H2
- Oxígeno: O2
- Nitrógeno: N2
- Fósforo: P
También los halógenos:
- Cloro: Cl
- Bromo: Br
-
Yodo: I
Los compuestos orgánicos se encuentran formando parte de la mayoría de sustancias que se encuentran en la tierra. Hacen parte constitutiva de los seres vivos formando moléculas de proteína, almidón, carbohidratos, lípidos, vitaminas y ácidos nucleicos entre otros.
La existencia de una gran variedad de compuestos orgánicos es dada por:
- La capacidad del átomo de carbono
para formar enlaces con otros átomos.
- La facilidad del átomo de carbono
para formar cadenas lineales, ramificadas, cíclicas con enlaces sencillos,
dobles o triples.
- El átomo de carbono, puede formar enlaces en tres dimensiones en el espacio debido a su estructura tetraedral.
1.2 Desarrollo
evolutivo de la química orgánica
La historia de la química se remonta hacia miles de años antes del origen de la vida, donde probablemente ya se producían reacciones orgánicas. Desde el descubrimiento del fuego, el hombre ha utilizado los compuestos orgánicos y sus reacciones, en:
- Cocinar los alimentos.
- Preparar pociones medicinales
de las plantas.
- Obtener sustancias para preparar
tintes de diferentes colores.
- Preparar bálsamos y aceites para ungir sus cuerpos.
La fuerza vital se inicia antes del siglo XIX, cuando se creía que los compuestos orgánicos se originaban de la materia viva, como las plantas, animales, motivo por el cual, existía una "fuerza vital" que diferenciaba los compuestos orgánicos de los inorgánicos.
- En el año 1814 al estudiar
los compuestos orgánicos se logra introducir la palabra isomería que significa
compuesto de partes iguales.
- Friedrich Wöhler (1828)
obtiene urea a partir de cianato de amonio. Los dos compuestos tienen la
misma fórmula molecular, es decir, son isómeros. Este concepto fue fundamental
para lograr el desarrollo de la teoría estructural.
- Se introduce a la química orgánica
el termino "radical". Paso fundamental en el entendimiento de los compuestos
orgánicos.
- Entre 1859 y 1860 un grupo de
científicos Kelulé, Couper y otros más concluyen la tetravalencia del carbono
y la formación de enlaces carbono carbono.
- Lothar Meyer (1830-1895),
denominó no saturados los compuestos que tenían doble enlace y reconoció
el triple enlace en el acetileno.
- C. W. Wilchelhaus, uso
el concepto de valencia, hecho de gran importancia para la química en general.
El concepto de valencia fue utilizado en un principio como el medio para
aclarar la naturaleza de los compuestos orgánicos.
- En (1874) Joseph Le Bel y otros científicos deducen la estructura tridimensional y los cuatro enlaces del átomo de carbono.
- El periodo comprendido entre1811 y 1905 se descubren aminas primarias (Charles Wurtz), se preparan alcoholes (Charles Friedel) y éteres a nivel de laboratorio (A. W. Williamson).
Pasa la Primera Guerra Mundial y la química orgánica avanza gradualmente en teorías electrónicas, instrumentación para separación e identificación de compuestos orgánicos. Se estudia la totalidad de las reacciones que se producen en los seres vivos, con el fin de descubrir algún día el misterio de la vida.
En la actualidad se consideran cinco grandes divisiones:
- Química analítica.
- Química física.
- Química inorgánica.
- Química orgánica.
- Bioquímica.
1.3 El carbono
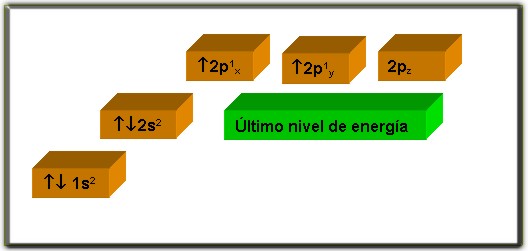
Es el átomo principal de los compuestos orgánicos, tiene la propiedad de unirse por medio de enlaces covalentes formando cadenas multicarbonadas. El carbono en su estado básico presenta seis electrones distribuidos de la siguiente forma:
1.3.1 Teoría de la hibridación
Formulada por el químico Linus Pauling y postula:
"En el momento de combinarse, los átomos alcanzan un estado de excitación, ganando energía. Como consecuencia los electrones saltan de un orbital inferior a uno superior".
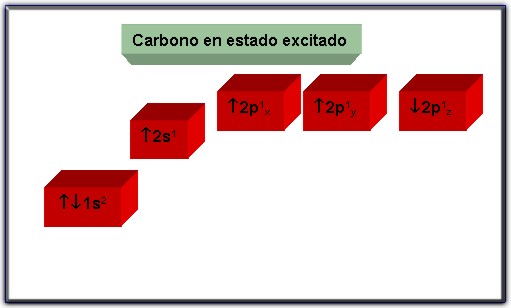
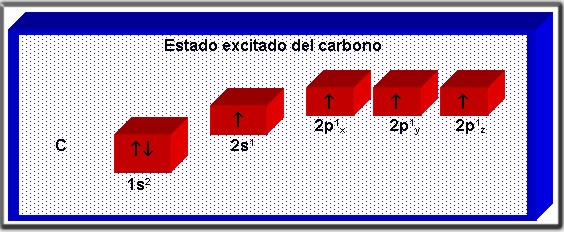
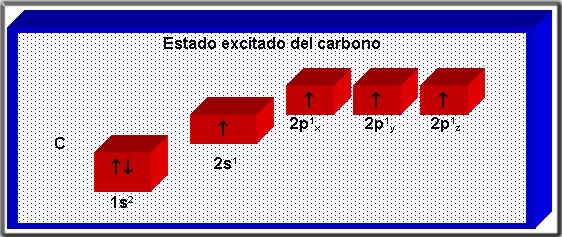
1.3.2 Estado excitado del carbono
Cuando el estado fundamental del carbono adquiere energía el electrón del orbital 2s salta al orbital 2pz, que se encontraba vacío. Esto da lugar al estado excitado de carbono:
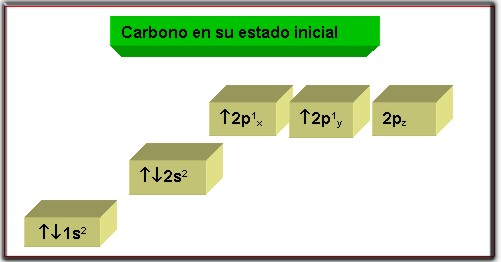
Al adquirir energía el carbono pasa al siguiente estado.
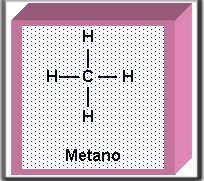
Al quedar electrones desapareados el carbono forma cuatro enlaces (tetravalente). En los enlaces formados hay diferencia de energía debido a que los orbitales p son más energéticos que los orbitales s. Experimentalmente, se ha comprobado que los cuatro enlaces que forma el carbono en el metano (CH4), son equivalentes, se necesita igual energía para romperlos.
1.3.3 Estado híbrido
del carbono
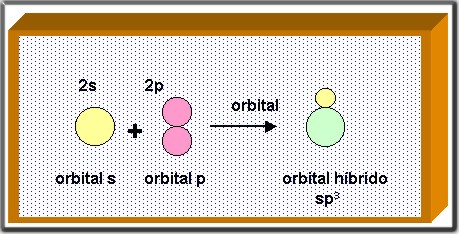
Se produce cuando se mezclan los orbitales s y p, el electrón del orbital 2s y los tres electrones del orbitale 2p suman sus energías y forman cuatro orbitales híbridos 2sp3; cada uno con características de s y de p, por esta razón se les denomina orbitales híbridos.
1.3.3.1 Hibridación sp3 tetragonal
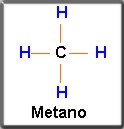
La hibridación sp3 o tetraedral le permite al carbono formar enlaces sencillos como es el caso de la molécula de metano.
La molécula de metano se obtiene porque cada orbital híbrido sp3 se superpone con el orbital 1s de cada hidrógeno, lo que equivale a que el electrón del orbital sp3 se una con el electrón del 1s, para formar un enlace de covalente sencillo.
Los orbitales s poseen una forma esférica y los orbitales p de ocho; cuando se mezcla o híbrida se obtiene también una forma de ocho, pero una de las mitades es mucho más grande que la otra.
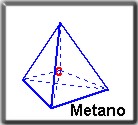
El orbital híbrido sp3 del carbono tiene una orientación espacial, lo que da origen a cuatro orbitales híbridos sp3 de este átomo, ellos se encuentran ubicados en los cuatro vértices de un tetraedro regular y en su punto central se ubica el núcleo del átomo de carbono. A este tipo de hibridación se le conoce como hibridación tetraedral o tetragonal.
1.3.3.2 Hibridación sp2
Mezcla entre un orbital s y dos orbitales p, el tercero conserva su forma pura.
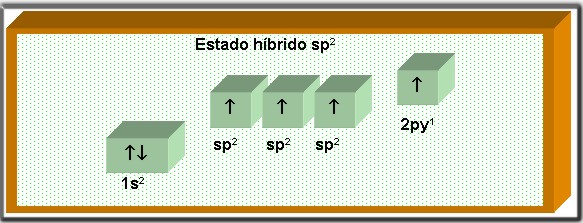
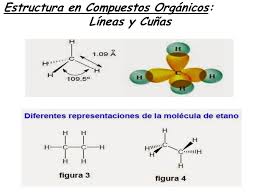
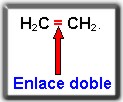
La hibridación sp2 se forman enlaces dobles, como en el eteno o etileno, al que le corresponde la siguiente estructura química:
1.3.3.3 Hibridación sp
Ocurre cuando el carbono excitado mezcla la energía del orbital 2s con un orbital p, los dos restantes conservan su forma pura.
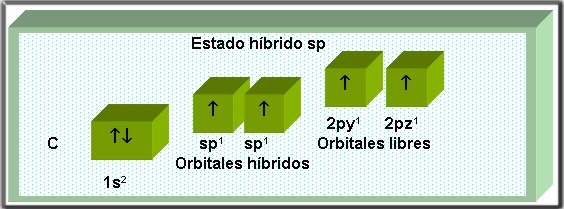
En este tipo de hibridación, se forman dos orbitales híbridos y dos puros. Dando origen a enlaces covalentes triples.
1.3.4 Clasificación
de los átomos de carbono
Los átomos de carbono se clasifican en:
- Primarios.
- Secundarios.
- Terciarios.
Es el átomo de carbono que se encuentra unido con otro.
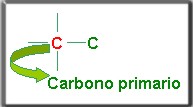
1.3.4.2 Carbono
secundario
Se encuentra unido con dos átomos de carbono.
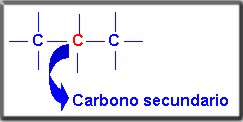
1.3.4.3 Carbono
terciario
Es aquel que se encuentra enlazado con tres átomos de carbono y se localiza en medio de ellos; es decir, que se encuentra rodeado por tres átomos.
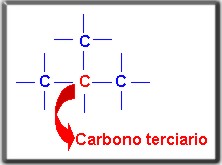
1.3.5 Importancia
del carbono
El carbono es el elemento representativo del grupo IV y de hecho este grupo se ha denominado familia del carbono. Además, es el más importante de los elementos de su grupo por ser el componente fundamental de los seres vivos formando compuestos orgánicos.
1.3.6 Formas alotrópicas del carbono
El carbono existe en tres formas alotrópicas:
- Diamante.
- Grafito.
- Carbono amorfo (Carbón vegetal, carbón animal, Hollín, coque).